LancetOncol研究揭秘HER2低表达乳腺癌的临床和分子特征
该文阐释4个创新性新远距放疗医学测试汇整预测科学研究,揭示HER2低抒发乳癌的医学和大分子特点。
抗体抗生素烯丙基物(ADC)等新型抗生素的出现重新表述了乳癌HER2抒发,并使得HER2低抒发成为一种捷伊乳癌血清型受到医学的重点关注。基于其明显的抗恶性肿瘤特异性,ADC抗生素有望成为HER2低抒发乳癌病人捷伊放疗优先选择。Lancet Oncol发表的一项科学研究透过汇整预测4个创新性新远距放疗医学测试的病人统计数据,意在比较HER2低抒发和HER2 0乳癌的医学和大分子特点,主要包括对新远距放疗的放疗化学反应和预后,以更好地描述HER2低抒发优点,从而帮助医学制定精确化的放疗决策。纳扎雷该科学研究介绍如下,概要。
科学研究背景及目地
HER2是一种CXCL10,也是能够显示HER2基因扩充以及相应HER2蛋白过抒发的乳癌和其他类型恶性肿瘤中具备较高化学反应率的放疗机理。如NSABP B-47测试右图,传统的抗HER2抗生素无法特别针对大多数HER2低或轻度抒发而无扩充的恶性肿瘤起到良好的放疗效果。然而,近些年来的医学测试结果显示,ADC抗生素等捷伊抗生素不仅特别针对典型HER2阴性乳癌具备医学特异性,特别针对HER2低或轻度抒发水平的恶性肿瘤同样具备明显医学特异性。
虽然这对于HER2低抒发乳癌是一大放疗突破,但是那些结果给医学病理也带来了挑战。目前医学病理主要集中于检验HER2过抒发恶性肿瘤[免疫系统诊断学(IHC)评分3+或IHC2 +/hybridization(ISH)阴性],虽然目前的HER2解译方式可以区分HER2全然阴性(IHC0)的恶性肿瘤与低(IHC1 +)或轻度抒发(IHC2 +/ISH阴性)的恶性肿瘤,但是IHC0与IHC1 +的区别并不具备医学有关性。出于实际目地,这三组经常被合并。因此,尚不清楚透过当前免疫系统诊断学方式检验到的HER2低抒发恶性肿瘤与否能代表具备确定恶性肿瘤生物化学优点的乳癌血清型。除此之外,IHC0与IHC1 +与否与早期乳癌新远距放疗的相同化学反应和相同存活期有关也是一个争论不休的问题。而回答那些问题对于进一步计划医学测试策略至关重要,主要包括靶向HER2低抒发恶性肿瘤放疗抗生素的优先选择以及形成更精确的HER2检验解译方式。
因此,科学人类学家透过评估在4项创新性医学测试(GeparSepto,NCT01583426;GeparOcto,NCT02125344;GeparX,NCT02682693;Gain-2,NCT01690702)中拒绝接受新远距放疗的病人堆栈的生物化学有关参数,主要包括激素蛋白(HR)状况、恶性肿瘤增殖、恶性肿瘤浸染白血球(TIL)和有关基因变异,意在验证HER2低抒发恶性肿瘤(IHC1 +或IHC2 +/ISH-)的生物化学和医学结局特点与否与HER2全然阴性恶性肿瘤(IHC0)相同。
科学研究方式
该汇整预测赞扬了4项创新性新远距放疗医学测试中由HER2非扩充继发性乳癌病人组成的堆栈,大部份病人均拒绝接受常规或强化剂量的以基因打靶抗生素-齿瓣烷为依据的放疗,且列入病人均未拒绝接受过抗HER2放疗。4个测试堆栈共主要包括3512例病人,其中2310例列入预测;排除HER2过抒发(IHC3 +)恶性肿瘤病人,仅列入参加Gain-2测试新远距放疗部分的病人。
在入组医学测试前,对大部份病人的HER2抒发状况进行了创新性标准化赞扬。根据美国医学恶性肿瘤专业委员会/美国病理家专业委员会(ASCO/CAP)指南,HER2低抒发表述为IHC1 +或IHC2 +/ ISH-,HER2 0表述为IHC0。
除此之外,还赞扬了激素蛋白(PR)、雄激素蛋白(ER)、Ki-67和TIL的抒发。根据国际TIL工作组的建议赞扬TIL。此等科学研究表明,TP53和PIK3CA的变异是乳癌常见的生物化学改变。为了预测恶性肿瘤中的那些变异,使用来自GeparSepto测试中556例HER2 0或HER2低抒发恶性肿瘤病人的新一代定序统计数据。在来自GeparOcto测试中549例病人的亚组堆栈中,可获得关于胚系BRCA1/2变异以及11个选定的乳癌易感基因(ATM,BARD1,TP53, BRIP1,CHEK2,FANCM,NBN,PALB2,RAD50,RAD51C,XRCC2)的统计数据。GeparOcto科学研究中没有显示TP53生殖系变异,因为该亚群中的大部份病人均为TP53WT。
科学研究共获得了1694例病人(来自除GeparX以外的大部份测试)的无病存活期(DFS)和总存活期(OS)统计数据,中位随访时间为46.6个月(IQR 35.0–52.3)。建立双变量和多变量logistic回归模型以及Cox比例风险模型,以预测科学研究终点病理全然缓解(pCR)、DFS和OS。
科学研究结果
基于HER2抒发和HR抒发的乳癌血清型在4项医学测试的3512例病人中的分布如图1右图。HER2过抒发恶性肿瘤病人从汇整预测中排除。
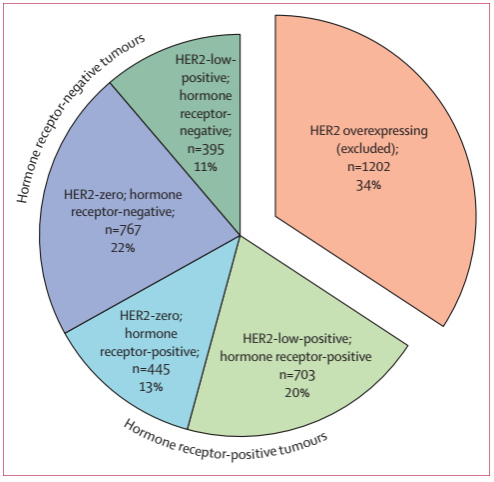 图1. 基于HR抒发和HER2抒发结合的乳癌改良分类
图1. 基于HR抒发和HER2抒发结合的乳癌改良分类在列入汇整预测的2310例病人中,1098例(47.5%)为HER2低抒发恶性肿瘤,1212例(52.5%)为HER2 0。GeparSepto、GeparOcto、Gain2和GeparX中HER2低抒发病人的百分比分别为492/810(60.7%)、209/563(37.1%)、137/321(42.7%)和260/616(42.2%)。在列入该汇整预测的病人中,GeparSepto测试中HR阴性病人的数量最多[534例(65.9%)/810例],相比之下,GeparOcto测试中为160例(28.4%)/563例,Gain2测试中为149例(46.4%)/321例,GeparX测试中为305例(49.5%)/616例。
在HR状况、增殖率(透过Ki-67测定)和分级方面,检验到HER2 0和HER2低抒发恶性肿瘤之间存在明显差异。在组织病理类型和淋巴结状况方面,观察到HER2 0(p=0.028)和HER2低抒发(p=0.0031)病人之间存在微小但明显的差异。观察到病人年龄作为连续变量而非分类变量存在明显差异;未观察到T分期和基质TIL存在差异。
在GeparSepto测试中拒绝接受新一代定序的556例恶性肿瘤中,HER2 0和HER2低抒发恶性肿瘤的PIK3CA变异率[209例中的34例(16.3%)vs 347例中的86例(24.8%),p=0.018]和TP53变异率[92例(44.0%)vs 116例(33.4%),p=0.012]存在明显差异。在HR阴性恶性肿瘤病人中,HER2 0和HER2低抒发亚组之间TP53变异率存在明显差异[49(38.0%)/129 vs 67(25.0%)/268,p=0.0078];然而,PIK3CA变异率无差异[31(24.0%)/129 vs 78(29.1%)/268;p=0.29]。在HR阴性恶性肿瘤病人中,未观察到TP53变异[43/80(53.8%)vs 49/79(62.0%),p=0.29]或PIK3CA变异[3/80(3.8%)vs 8/79(10.1%);p =0.11]在HER2 0和HER2低抒发亚组之间存在明显差异。
在GeparOcto测试中具备生殖系变异统计数据的549例病人中,HER2 0恶性肿瘤病人的BRCA1/2或其他乳癌易感基因的变异率明显高于HER2低抒发恶性肿瘤病人[92(26.8%)/343 vs 39(18.9%)/206,p= 0.039];在HR阴性和HR阴性亚组中观察到相似结果,但不具备明显性。
在pCR率方面,HER2低抒发恶性肿瘤病人的pCR率明显低于HER2 0恶性肿瘤病人(图2A)。双变量logistic回归预测与该预测一致(图2B,D)。然而,在多变量预测中,pCR率无差异(图2C,E)。在HR阴性恶性肿瘤中,HER2低抒发恶性肿瘤病人的pCR率明显低于HER2 0恶性肿瘤病人(图2A)。在HR阴性恶性肿瘤中,未观察到相同HER2抒发状况的pCR率差异(图2A)。在双变量logistic回归预测和多变量logistic回归预测中观察到相似的结果(图2B、C、D、E)。未观察到HER2 IHC1 +与HER2 IHC2 +恶性肿瘤之间pCR率的任何差异。
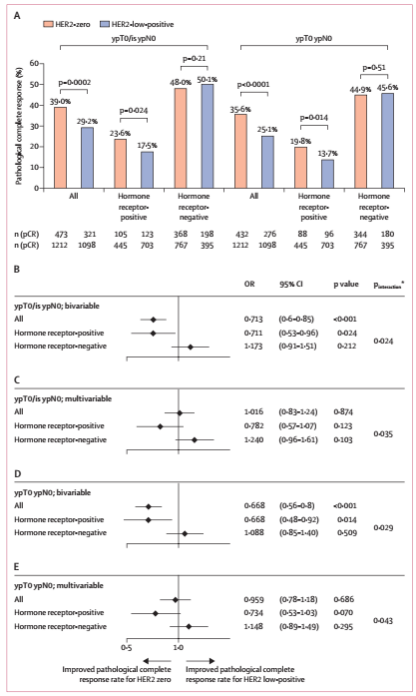 图2. HER2 0和HER2低抒发乳癌的pCR率
图2. HER2 0和HER2低抒发乳癌的pCR率HER2低抒发恶性肿瘤病人的DFS[3年DSF率:83.4%(95%CI:80.5-85.9)vs 76.1%(72.9-79.0);分层对数秩检验p=0.0084]和OS[3年OS率:91.6%(84.9-93.4)vs 85.8%(83.0-88.1);分层对数秩检验p=0.0016;(图3A,B)]明显优于HER2 0恶性肿瘤病人;HR阴性恶性肿瘤病人亚组也是如此[3年DFS率:84.5%(79.5-88.3)vs 74.4%(70.2-78.0);分层对数秩检验p=0.0076;3年OS率:90.2%(86.0-93.2)vs 84.3%(80.7-87.3);分层对数秩检验p=0.016;(图3E,F)]。然而,HR阴性恶性肿瘤中相同HER2抒发状况的存活期无差异[3年DFS率:HER2低抒发组为82.8%(95%CI:79.1-85.9),HER2 0组为79.3%(73.9-83.7);分层对数秩检验p=0.39;3年OS率:92.3%(89.6-94.4)和88.4%(83.8-91.8);分层对数秩检验p=0.13;(图3 C、D)]。双变量和多变量预测的结果与单变量预测一致(图4)。未观察到HER2 IHC1 + 与HER2 IHC 2 + 恶性肿瘤病人之间的DFS或OS存在任何差异。
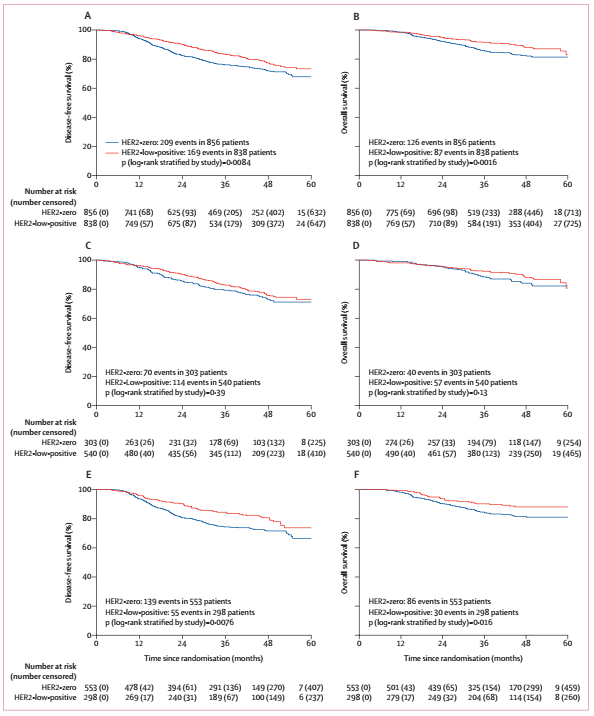 图3. DFS和OS的Kaplan-Meier生存预测
图3. DFS和OS的Kaplan-Meier生存预测在HR阴性恶性肿瘤且未获得pCR的病人中,按病理全然缓解状况(使用ypT0/is ypN0表述)对DFS和OS进行界标预测,结果显示HER2低抒发和HER2 0恶性肿瘤之间存在明显差异[3年DFS率:79.0% (95%CI:71.3–84.8)vs 63.4%(95%CI:57.4–68.8);分层对数秩检验p=0.0023;3年OS率:86.6%(79.8–91.2)vs 75.7%( 70.1–80.5);分层对数秩检验p=0.0078]。在双变量和多变量Cox回归预测中观察到相似的结果。然而,在HR阴性恶性肿瘤且获得pCR的病人中,HER2低抒发和HER2 0恶性肿瘤之间未见差异[3年DFS率90.6%(95%CI:84.0–94.6)vs 88.5%(95%CI:83.3–92.1),分层对数秩检验p=0.63;3年OS率94.3%(88.4–97.3)vs 95.3%(91.4–97.5);分层对数秩检验p=0.45]。不考虑病理全然缓解状况,在HR阴性恶性肿瘤病人中未观察到相同HER2状况的DFS或OS存在明显差异。
科学研究总结及思考
本科学研究赞扬了4个医学测试的联合堆栈统计数据,以检验HER2 0和HER2低抒发恶性肿瘤之间的差异。结果显示HER2 0和HER2低抒发恶性肿瘤属于相同的生物化学血清型,具备相同的医学病理特点,主要包括HR抒发差异、HR阴性恶性肿瘤的pCR率差异,以及HR阴性恶性肿瘤的生存差异。由于HR信号转导和HER2信号转导之间存在交叉化学反应,HER2低抒发可能是HR阴性乳癌的放疗抵抗因素。
该科学研究表明对于获得pCR的病人,无论HER2 0还是HER2低抒发恶性肿瘤病人,其预后均非常好。然而科学研究还发现,HR阴性、HER2 0恶性肿瘤的pCR率较高并不能转化为HR阴性亚组的生存差异。其他生物标志物也观察到这一发现,典型的例子是Ki-67,它是pCR的阴性预测因子,同时也是生存的不良预后因素。在这种情况下,高Ki-67水平的恶性肿瘤具备更强的侵袭性生物化学优点,这就解释了HR阴性、HER2 0病人pCR率高和生存率低的原因。
并且,未获得pCR的HR阴性、HER2低抒发乳癌病人的预后优于HR阴性HER2 0乳癌,但应强调的是,该预后仍比获得pCR病人的预后差很多。因此,仍存在透过靶向放疗HER2低抒发恶性肿瘤以改善该亚组病人预后的医疗需求。新一代ADC抗生素因为具备旁观者效应,其释放的亲脂性载药能跨膜进入临近恶性肿瘤细胞,即使那些细胞并不抒发靶抗原,因而特别针对HER2低抒发乳癌也能发挥强效抗恶性肿瘤作用,值得进一步探索以满足HER2低抒发乳癌病人的放疗需求。
参考文献:
[1]Denkert C, Seither F, Schneeweiss A, et al. Clinical and molecular characteristics of HER2-low-positive breast cancer: pooled analysis of individual patient data from four prospective, neoadjuvant clinical trials. Lancet Oncol. 2021 Aug;22(8):1151-1161.
审批编号:CN-90310
有效期至:2023-1-20
排版:王璐
编辑:王璐
审核:祁晓梦
相关文章
发表评论
评论列表
- 这篇文章还没有收到评论,赶紧来抢沙发吧~


